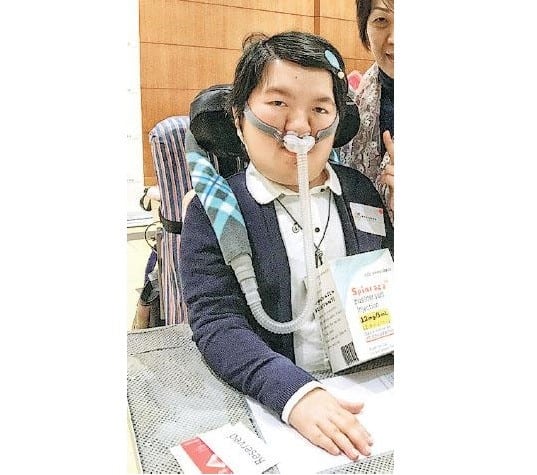
罕見病脊髓肌肉萎縮症(Spinal Muscular Atrophy, 簡稱SMA)患者周佩珊(圖),去年10月向特首林鄭月娥陳情後,政府早前與美國藥廠達成共識,引入新藥。首批可用藥的11名第一型(即病情最嚴重)患者中,已有兩名約兩歲的小童開始用藥,周佩珊母親表示女兒要先接受脊髓手術後才可用藥,「現在要她增肥應付手術,急不來」。
最小者先 周佩珊最後
食物及衛生局長陳肇始上月中公布港府引入新藥,並透過「特別用藥計劃」,於上月9日免費為首名經臨牀評估為合適的第一型患者注射第一劑藥物,瑪麗醫院陸續安排相關患者用藥。
周佩珊母親昨向本報表示,首批有11名第一型患者、包括佩珊可獲用藥。據她所知,用藥安排由年紀最小的患者開始,目前兩名約兩歲的病童已開始用藥,分別接種了第2及第3劑,而現年23歲的佩珊應排在最後一位。
佩珊要先增肥 脊骨開洞
周太說,佩珊曾接受植骨手術,脊髓空隙被「骨水泥」填滿,需接受全身麻醉手術在脊骨開洞,才能用藥,暫未知手術時間。周太說,在港大就讀的佩珊已考完試,現時首要目標是增肥應付脊骨手術,用藥一事「急不來」。
SMA藥物有望今年底在港註冊,不同類型的患者如適合用藥,可透過關愛基金資助陸續接受治療。另一名患者的母親Carol說,11歲兒子屬SMA第三型,並非首批可用藥的患者,她較關注即將出台的關愛基金病人藥物分擔機制。
有家屬憂關愛分擔機制
她說藥物獲註冊後,所有用藥患者包括佩珊都要申請關愛基金支付藥費,若分擔機制未能維持病人原本的生活水平,甚至要傾家蕩產的話,她不排除有父母會為降低資產總額而選擇離婚,以支付較少藥費。
內地制罕見病名錄 港未有
此外,內地衛生健康委員會等5個部門聯合制定的《第一批罕見病名錄》於上月底出台,涵蓋121種罕見病,包括脊髓肌肉萎縮症、黏多醣症、多發性硬化症等。另國家醫政管理局制定《罕見病目錄制定工作程序》,定期更新有關名錄,又列明納入名錄需符合病發率低、對患者危害大、有明確診斷方法,以及未有有效治療方法但納入國家科研專項等,罕見病團體等可向專家委員會提交建議。
香港罕見疾病聯盟會長曾建平說,內地民間團體可自下而上申請將罕見病納入名錄,比香港優勝。他早前已就內地訂立名冊去信林鄭月娥,他認為政府應有承擔,「不可能要每一種病的患者都走到電視前講出訴求」。他說當局已回覆指交由食衛局跟進。
食衛局發言人稱,國際間對不常見疾病並無一致定義, 在現行醫療政策下,每名到公立醫院接受醫療服務的病人均有同等機會接受治療。